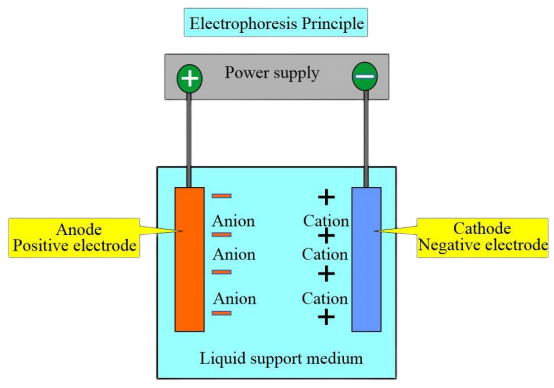
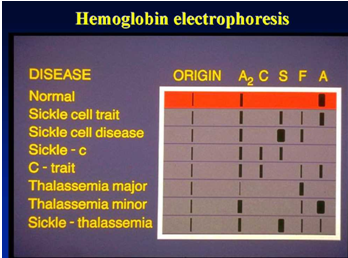
Principiul experimentului
Electroforeza hemoglobinei are ca scop detectarea și confirmarea diferitelor hemoglobine normale și anormale.
Datorită sarcinilor și punctelor izoelectrice diferite ale diferitelor tipuri de hemoglobină, într-o anumită soluție tampon de pH, atunci când punctul izoelectric al hemoglobinei este mai mic decât pH-ul soluției tampon, hemoglobina poartă o sarcină negativă și migrează către anod în timpul electroforezei. În schimb, hemoglobina cu sarcină pozitivă se deplasează spre catod.
Sub o anumită tensiune și după un anumit timp de electroforeză, hemoglobinele cu sarcini și greutăți moleculare diferite prezintă direcții și viteze de migrare diferite. Acest lucru permite separarea zonelor distincte, iar analizele ulterioare de scanare colorimetrică sau electroforetică pot fi efectuate pe aceste zone pentru a cuantifica diferite hemoglobine. Cea mai des folosită metodă este electroforeza membranei cu acetat de celuloză cu pH 8,6.
În citoplasmă, grupările etilenglicol (CHOH-CHOH) prezente în substanțele glicogenate sau polizaharide (cum ar fi mucopolizaharide, mucoproteine, glicoproteine, glicolipide etc.) sunt oxidate de acidul periodic și transformate în grupări aldehidice (CHO-CHO). Aceste grupări aldehide se combină cu reactivul Schiff incolor roșu-violet, formând un colorant roșu-violet care se depune acolo unde polizaharidele sunt prezente în celulă. Această reacție este cunoscută sub denumirea de colorare periodică acid-Schiff (PAS), denumită anterior colorare cu glicogen.
Metoda de experiment
Materiale:Acetat de celulozămembrană, aparat de electroforeză(DYCP-38C și sursă de alimentare DYY-6C), Instrument superior de încărcare a mostrelor (pipetă), spectrofotometru, cuve colorimetrice, tampoane.
Tampon:
(1) Tampon pH 8,6 TEB: Se cântăresc 10,29 g Tris, 0,6 g EDTA, 3,2 g acid boric și se adaugă apă distilată la 1000 ml.
(2) Tampon borat: Se cântăresc 6,87 g borax și 5,56 g acid boric și se adaugă apă distilată la 1000 ml.
Procedură:
Prepararea soluției de hemoglobină
Luați 3 ml de sânge care conține heparină sau citrat de sodiu ca anticoagulant. Se centrifugă la 2000 rpm timp de 10 minute și se aruncă plasma. Spălați globulele roșii de trei ori cu soluție salină fiziologică (750 rpm, 5 minute centrifugare de fiecare dată). Se centrifugă la 2200 rpm timp de 10 minute și se aruncă supernatantul. Adăugați o cantitate egală de apă distilată, apoi adăugați de 0,5 ori volumul de tetraclorură de carbon. Agitați energic timp de 5 minute, apoi centrifugați la 2200 rpm timp de 10 minute pentru a colecta soluția superioară de Hb pentru utilizare ulterioară.
Înmuierea membranei
Tăiați membrana de acetat de celuloză în benzi de 3 cm × 8 cm. Înmuiați-le în tampon cu pH 8,6 TEB până când sunt complet saturate, apoi îndepărtați și ștergeți-le cu hârtie de filtru.
Spotting
Folosiți o pipetă pentru a localiza 10 μl de soluție de hemoglobină vertical pe membrana de acetat de celuloză (partea aspră), la aproximativ 1,5 cm de margine.
Electroforeză
Se toarnă soluția tampon de borat în camera de electroforeză. Așezați membrana de acetat de celuloză cu partea pătată la capătul catodic al camerei. Rulați la 200 V timp de 30 de minute.
Eluare
Tăiați zonele HbA și HbA2, puneți-le în eprubete separate și adăugați 15 ml și, respectiv, 3 ml apă distilată. Agitați ușor pentru a elua hemoglobina complet, apoi amestecați.
Colorimetrie
Se pune la zero absorbanța folosind apă distilată pentru soluția de eluție și se măsoară absorbanța la 415 nm.
Calcul
HbA2(%) = Absorbanța tubului HbA2 / (Absorbanța tubului HbA × 5 + Absorbanța tubului HbA2) × 100%
Calculul rezultatelor experimentale
Interval de referință pentru pH 8,6 TEB tampon electroforeză acetat de celuloză: HbA > 95%, HbA2 1%-3,1%
Note
Timpul de electroforeză nu trebuie să fie prea lung. Membrana de acetat de celuloză nu trebuie să se usuce în timpul electroforezei. Opriți electroforeza atunci când HbA și HbA2 sunt clar separate. Electroforeza prelungită poate provoca difuzia benzii și estomparea.
Evitați utilizarea prea multă probă. Lichidul excesiv de hemoglobină poate duce la desprinderea benzii sau la o colorare insuficientă, ceea ce duce la niveluri fals crescute de HbA.
Preveniți contaminarea membranei de acetat de celuloză cu proteine.
Curentul nu trebuie să fie prea mare; în caz contrar, benzile de hemoglobină pot să nu se separe.
Includeți întotdeauna specimene de la indivizi normali și hemoglobinele anormale cunoscute necesare ca martori.
Beijing Liuyi Biotechnology produce rezervorul profesional de electroforeză pentru electroforeza hemoglobinei care este modelulDYCP-38CRezervor de electroforeză cu membrană de acetat de celuloză și există două modele de surse de alimentare pentru electroforeză disponibile pentru rezervorul de electroforeză cu membrană de acetat de celulozăDYY-2CşiDYY-6Calimentare electrică.
Între timp, Beijing Liuyi Biotechnology oferă clienților membrană de acetat de celuloză, iar dimensiunea membranei de acetat de celuloză poate fi personalizată. Bine ați venit să ne cereți mostre și mai multe informații.
Marca Beijing Liuyi are o istorie de peste 50 de ani în China, iar compania poate oferi produse stabile și de înaltă calitate în întreaga lume. Prin ani de dezvoltare, este demn de alegerea ta!
Acum căutăm parteneri, atât rezervorul de electroforeză OEM, cât și distribuitorii sunt bineveniți.
Dacă aveți vreun plan de achiziție pentru produsele noastre, vă rugăm să nu ezitați să ne contactați. Ne puteți trimite mesaj pe e-mail[email protected]sau[email protected], sau vă rugăm să ne sunați la +86 15810650221 sau adăugați Whatsapp +86 15810650221 sau Wechat: 15810650221
Ora postării: 20-sept-2023